引用信息 |
文 章:Supramolecular lipid nanoparticle reprograms tumor microenvironment by cucurbit[7]uril-based host–guest recognition for STING-activating cancer immunotherapy. 期 刊:Materials Today(影响因子:22) 发表时间:2025年12月3日 作 者:Shaolong Qi, Xueyan Zhang, Xinyang Yu, et al. 作者单位:清华大学 使用产品:Mouse IL-1β ELISA kit 文章链接:https://www.sciencedirect.com/science/article/abs/pii/S1369702125004870 |

靶向cGAS-STING通路为癌症免疫治疗提供了机会,然而,实体瘤的临床治疗效果仍不尽如人意。最新证据表明,免疫抑制性肿瘤微环境(TME)严重阻碍了T细胞的活化、增殖和浸润。“冷肿瘤”(cold tumor)的免疫原性降低,会显著削弱免疫系统对肿瘤细胞的杀伤能力,从而复杂化细胞毒性(cytotoxicity)的实现,且小分子STING激动剂在体内被迅速代谢,导致其半衰期缩短,加快了从体内的清除速度,从而大大削弱了抗肿瘤效果。此外,肿瘤内源性多胺的积累显著抑制了cGAS活性,进一步降低了基于STING的免疫治疗的治疗效果。为应对这些挑战,本研究开发了一种超分子脂质纳米颗粒系统(MC7-LNP),旨在重编程免疫抑制性TME并增强STING激动剂的治疗效果。MC7-LNP平台通过主客体识别和金属配位同时结合了MSA-2和铜离子。一种经修饰的葫芦[7]脲基脂质促进了MSA-2在肿瘤细胞中的持续释放,并限制了内源性多胺的功能。同时,铜离子诱导的氧化应激促进了受损DNA和损伤相关分子模式的形成,显著增强了肿瘤细胞的免疫原性并恢复了T细胞功能。结合编码免疫刺激性细胞因子IL-12的mRNA,这种创新的超分子方法显著抑制了黑色素瘤的进展,并引发了强烈的细胞毒性T淋巴细胞反应。该研究结果提供了一种有前景的协同模式,通过重塑TME来增强基于STING激动剂的免疫疗法。
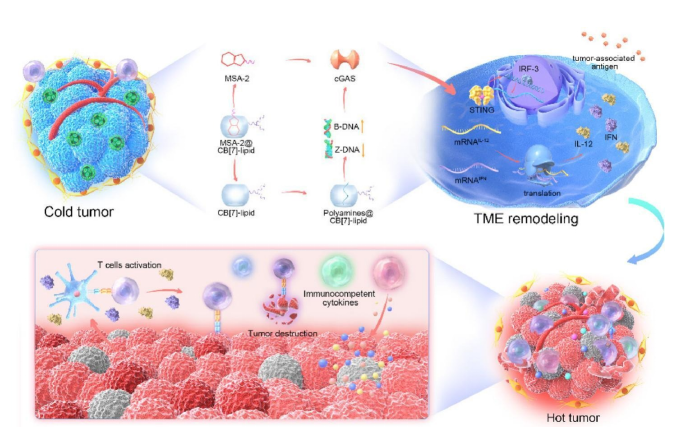
图示:基于葫芦[7]脲与MSA-2之间的主客体识别作用开发的超分子脂质纳米颗粒系统,旨在重编程免疫抑制性肿瘤微环境(TME),并增强STING激活免疫疗法的疗效。该方法与mRNAIL-12联合使用,在黑色素瘤模型中表现出优异的抗肿瘤效果,并通过将“冷肿瘤”转化为“热肿瘤”,激发了强烈的细胞毒性T淋巴细胞反应。
引用文献
Shaolong Qi, Xueyan Zhang, Xinyang Yu, et al. Supramolecular lipid nanoparticle reprograms tumor microenvironment by cucurbit[7]uril-based host–guest recognition for STING-activating cancer immunotherapy. Materials Today. Volume 92, January–February 2026, Pages 101-114.
相关产品
该项研究中,使用了欣博盛生物(NeoBioscience Technology Co, Ltd)的Mouse IL-1β ELISA试剂盒,用于检测相关因子的含量。
货号 | 产品名称 | 灵敏度 | 检测范围 |
EMC001b | QuantiCyto® Mouse IL-1β ELISA kit | 7.8 pg/ml | 15.6-1000 pg/ml |


