| 引用信息 |
| 文 章:mRNA-Based Vaccination Drives in Vivo Dendritic Cell Reprogramming and Selective Cytotoxic T Lymphocyte Modulation for Enhanced Antitumor Immunity. 期 刊:ACS Nano(影响因子:16) 发表时间:2025年10月28日 作 者:Chenshuang Zhang, William Stewart, Yilong Teng, et al. 作者单位:上海交通大学 使用产品: Mouse IL-6、TNF-α和IFN-γ ELISA kits 文章链接:https://pubs.acs.org/doi/10.1021/acsnano.5c09365?goto=supporting-info |

精确工程化改造T细胞以实现靶向肿瘤识别,并克服体内抗原特异性T细胞不足的问题,是癌症免疫治疗中的主要挑战。本研究提出了一种名为VISIT(疫苗诱导的选择性T细胞调节)的简化策略,该策略通过体内树突状细胞(DC)重编程实现对细胞毒性T淋巴细胞(CTLs)的时空调节。该方法采用经优化的脂质纳米颗粒,将编码肿瘤抗原以及膜结合型IL 15/IL 15Rα复合物(bIL 15,为IL 15的生物活性形式)的mRNA选择性递送至脾脏DC。系统给药后,VISIT平台成功实现DC的体内重编程,使其同步在细胞表面呈现抗原/MHC I复合物与bIL 15。这个“一石二鸟”的设计可同时向CD8⁺ T细胞反式呈递肿瘤抗原和bIL 15,从而在有效促进抗原特异性CTL原位生成与扩增、推动肿瘤清除和免疫记忆建立的同时,最大程度避免了非特异性免疫激活的风险。
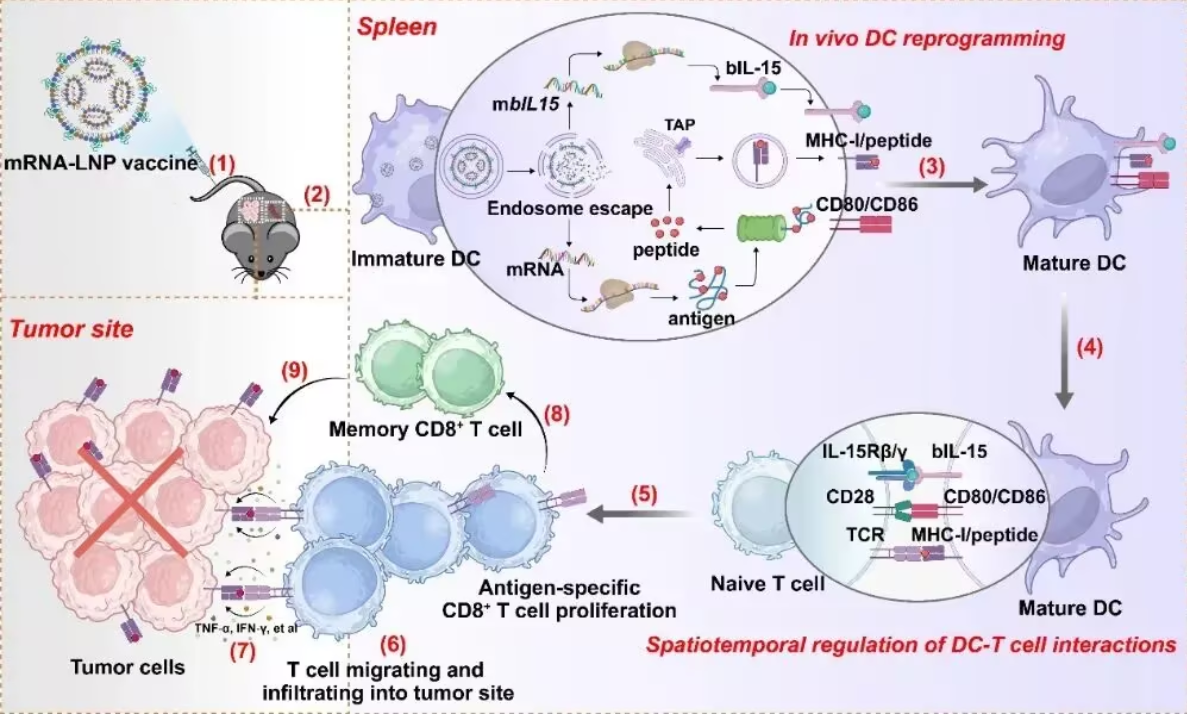
VISIT平台通过体内DC重编程引发强烈的抗原特异性T细胞免疫反应的示意图
体内实验表明,mRNA-LNP疫苗经全身给药后,在脾脏实现了96%的编码蛋白表达效率,并成功转染约33%的DC。进一步机制研究显示,VISIT策略不仅能促进DC成熟与抗原提呈,还可程序化地将bIL-15定向递送至抗原特异性CD8⁺ T细胞,从而显著增强CTL扩增与抗原特异性体液免疫应答。在预防性接种实验中,该疫苗完全抑制肿瘤生长,并诱导长效记忆T细胞反应,实现对肿瘤再攻击的有效防护。在MC38-OVA结肠癌模型与高侵袭性B16F10黑色素瘤模型中,治疗性接种均显著增强CTL应答,有效延缓肿瘤进展并延长生存期。尤为重要的是,该疫苗与免疫检查点抑制剂联用表现出协同抗肿瘤效应,进一步提升了黑色素瘤模型的治疗效果。
综上,VISIT疫苗平台通过精准时空调控DC与T细胞间相互作用,为发展个性化癌症免疫治疗提供了全新的体内DC重编程策略。该平台不仅为个体化免疫治疗提供了通用型技术路径,也有望成为过继性T细胞疗法的有效协同方案。
引用文献
Chenshuang Zhang, William Stewart, Yilong Teng, et al. mRNA-Based Vaccination Drives in Vivo Dendritic Cell Reprogramming and Selective Cytotoxic T Lymphocyte Modulation for Enhanced Antitumor Immunity. ACS Nano.2025 Nov 11;19(44):38267-38283..
相关产品
该项研究中,使用了欣博盛生物(NeoBioscience Technology Co, Ltd)的Mouse IL-6、TNF-α和IFN-γ ELISA试剂盒,用于检测细胞培养上清液中的相关因子含量。
货号 | 产品名称 | 灵敏度 | 检测范围 |
QuantiCyto® Mouse IL-6 ELISA kit | 7.8 pg/ml | 15.6-1000 pg/ml | |
QuantiCyto® Mouse TNF-α ELISA kit | 15.6 pg/ml | 31.25-2000 pg/ml | |
QuantiCyto® Mouse IFN-γ ELISA kit | 3.9 pg/ml | 7.8-500 pg/ml |


