引用信息 |
文 章:Lactobacillus extracellular vesicle-driven oxygen-releasing photothermal hydrogel reprograms macrophages and promotes angiogenesis to accelerate diabetic wound healing. 期 刊:Bioactive Materials(影响因子:20.3) 发表时间:2025年8月15日 作 者:Pingyun Yuan, Meng Deng , Xueru Li, et al. 作者单位:西北有色金属研究院&西安组织工程与再生医学研究&西安交通大学第二附属医院 使用产品: Mouse TNF-α和IL-10 ELISA kits 文章链接:https://www.sciencedirect.com/science/article/pii/S2452199X25003639 |

慢性伤口愈合在临床上仍具有挑战性,原因在于血管生成不足且伴有持续的炎症微环境。巨噬细胞M2极化在消除炎症和促进血管生成中发挥着关键作用。利用可扩展性和转化优势,本研究采用源自保加利亚乳杆菌的细胞外囊泡(Lactobacillus bulgaricus,Lac-EVs),开发了一种基于壳聚糖(CS)的光热水凝胶(PCPH@Lac-EVs),用于高效递送Lac-EVs,以协同解决糖尿病伤口愈合过程中血管新生不足与持续炎症的难题。该水凝胶通过席夫碱交联反应制备,具备良好的自愈性能、组织粘附性和生物相容性,可贴合不规则创面并实现Lac-EVs的持续释放。此外,PCPH@Lac-EVs能够补充氧气,并在近红外(NIR)照射下发挥光热效应。体外研究表明, PCPH@Lac-EVs可有效诱导M2巨噬细胞极化,增强内皮细胞迁移,并促进血管生成。在糖尿病小鼠全层皮肤缺损模型中,PCPH@Lac-EVs联合NIR照射在13天内实现了99.3%的伤口闭合率,显著优于未处理的对照组(72.3%)。机制研究发现,愈合加速源于氧气释放与温和光热刺激共同作用,协同增强Lac-EVs介导的免疫调节与功能型血管新生,从而显著促进糖尿病伤口修复。
该研究通过构建一种多功能水凝胶递送系统,有效克服了Lac-EVs在糖尿病伤口治疗中的递送瓶颈,显著增强了其疗效。该系统不仅提高了Lac-EVs的生物利用度,还通过氧气释放和光热刺激进一步增强了其抗炎和促血管新生的能力,为糖尿病伤口治疗提供了一种具有临床转化潜力的新策略。
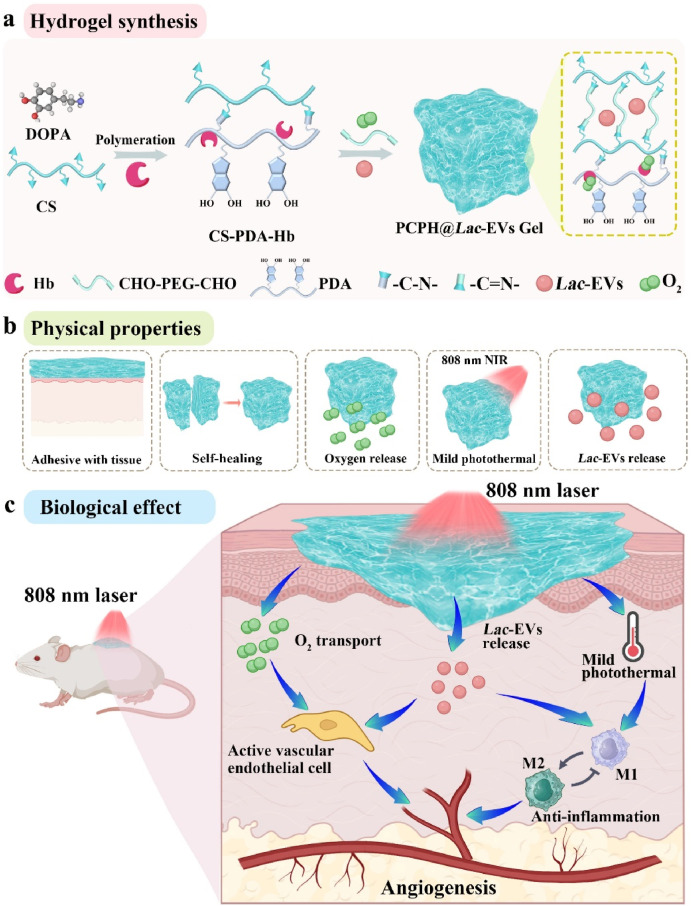
方案1.(a) 可注射PCPH@Lac-EVs水凝胶的合成示意图。(b) PCPH@Lac-EVs水凝胶的物理性能展示。(c) PCPH@Lac-EVs水凝胶通过供氧、缓慢释放Lac-EVs以及产生温和光热效应促进糖尿病伤口愈合的机制示意图
引用文献
Lactobacillus extracellular vesicle-driven oxygen-releasing photothermal hydrogel reprograms macrophages and promotes angiogenesis to accelerate diabetic wound healing. Bioactive Materials. Volume 54, December 2025, Pages 144-158.
相关产品
该项研究中,使用了欣博盛生物(NeoBioscience Technology Co, Ltd)的 Mouse TNF-α和IL-10 ELISA试剂盒,用于检测细胞培养上清液中的相关指标含量。
货号 | 产品名称 | 灵敏度 | 检测范围 |
QuantiCyto® Mouse TNF-α ELISA kit(小鼠肿瘤坏死因子-α) | 15.6 pg/ml | 31.25-2000 pg/ml | |
QuantiCyto® Mouse IL-10 ELISA kit(小鼠白细胞介素-10) | 1.95 pg/ml | 3.9-250 pg/ml |


